有機ホウ素・有機ケイ素化合物は、有機合成化学において幅広く利用されています。これら有機金属反応剤は高い安定性を持ちながら、適切な試薬や遷移金属触媒により活性化され、多様な反応性を示します。また,それら有機化合物そのものが,医薬品や機能性有機材料として有用であることも明らかにされています。しかし、高度に官能基化された有機ホウ素・有機ケイ素化合物の合成は未だ困難であり、新しい選択的合成法の開発が求められています。
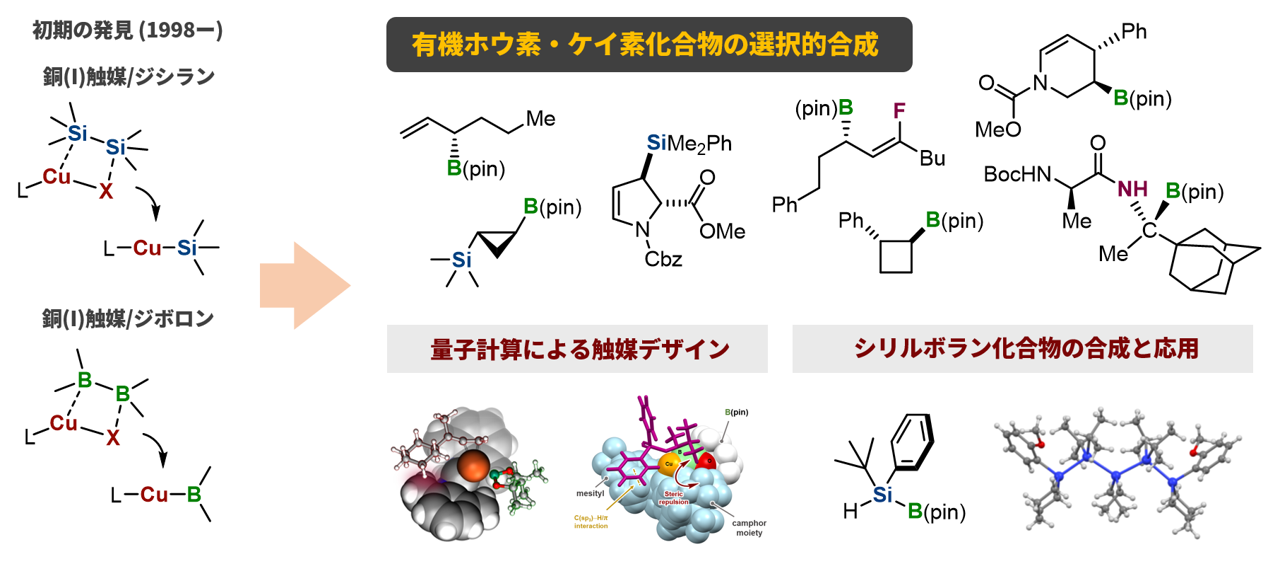
有機ケイ素化合物と有機ホウ素化合物の新しい合成法
私たちは1998年に、銅(I)触媒を用いたジシラン化合物をケイ素化剤とする求核的ケイ素化反応を発見しました。さらにケイ素化合物とホウ素化合物は遷移金属に対する反応性が似ていることを手がかりに、銅(I)触媒を用いたジボロン化合物をホウ素化剤とする反応を検討したところ、共役カルボニル化合物への付加反応が進行することも見つけました。これらの発見を手がかりに、有機ホウ素・ケイ素化合物の新しい合成法を数多く開発することに成功しました。さらに最近では、量子化学計算を駆使したキラル銅(I)触媒の合理的設計、ならびにケイ素求核剤の前駆体として働くシリルボラン化合物の一般的合成法の開発にも成功しました。今後も有機ホウ素および有機ケイ素化学の限界を押し広げるべく、研究を進めています。
研究紹介記事
- “計算化学による合理的設計で高性能なキラル触媒を開発 ~60 年におよぶ未解決課題を計算と実験で解決~”
『北海道大学プレスリリース』 (2018/6/12)
- “量子化学計算を駆使した不斉ホスフィン配位子設計から導かれる新たな不斉ホウ素化反応”
『Chem-Station スポットライトリサーチ』 (2018/8/27)
- “ケトンの不斉ホウ素化反応の開発に初めて成功”
『北海道大学プレスリリース』 (2017/5/10)
- “インドールの触媒的不斉ヒドロホウ素化反応の開発”
『Chem-Station スポットライトリサーチ』 (2016/1/8)
- “銅(Ⅰ)錯体触媒による合成反応開発と発光性金(Ⅰ)錯体の動的挙動 : 偶然の発見が自分の研究の幅を広げてくれました!”
『化学と工業』 2014年9月号、793-795ページ。
- “銅触媒による有機ホウ素化合物の新合成法とメカノ応答性をもつ発光性金錯体の開発”
『化学と工業』 2014年3月号、201ページ。
- “求核的ホウ素-金属化学種の新展開 : 含ホウ素化合物の革新的合成法をもたらす新活性種”
『化学と工業』 2008年3月号、224-225ページ。
代表的な論文
- Conformationally Fixed Chiral Bisphosphine Ligands by Steric Modulators on the Ligand Backbone: Selective Synthesis of Strained 1,2-Disubstituted Chiral cis-Cyclopropanes.
Iwamoto, H.; Ozawa, Y.; Hayashi, Y.; Imamoto, T.; Ito, H.* J. Am. Chem. Soc. 2022, 144, 10483–10494.
DOI: 10.1021/jacs.2c02745
- Regio- and Stereoselective Synthesis of Multi-Alkylated Allylic Boronates through Three-Component Coupling Reactions between Allenes, Alkyl Halides, and a Diboron Reagent.
Ozawa, Y.; Endo, K.; Ito, H.* J. Am. Chem. Soc. 2021, 143, 13865–13877.
DOI: 10.1021/jacs.1c06538
- Synthesis of Hydrosilylboronates via the Monoborylation of a Dihydrosilane Si−H Bond and Their Application for the Generation of Dialkylhydrosilyl Anions.
Takeuchi, T.; Shishido, R.; Kubota, K.*; Ito, H.* Chem. Sci. 2021, 12, 11799–11804.
DOI: 10.1039/D1SC01440D
- A Copper(I)-Catalyzed Radical Relay Reaction Enabling the Intermolecular 1,2-Alkylborylation of Unactivated Olefins
Akiyama, S.; Oyama, N.; Endo, T.; Kubota, K.; Ito, H.* J. Am. Chem. Soc. 2021, 143, 5260–5268.
DOI: 10.1021/jacs.1c02050
- General Synthesis of Trialkyl- and Dialkylarylsilylboranes: Versatile Silicon Nucleophiles in Organic Synthesis
Shishido, R.; Uesugi, M.; Takahashi, Rikuro.; Mita, T.; Ishiyama, T.; Kubota, K.*; Ito, H.* J. Am. Chem. Soc. 2020, 142, 14125–14133.
DOI: 10.1021/jacs.0c03011
- Computational Design of High-performance Ligand for Enantioselective Markovnikov Hydroboration of Aliphatic Terminal Alkenes.
Iwamoto, H.; Imamoto, T.; Ito, H.* Nature Commun. 2018, 9, 2290.
DOI: 10.1038/s41467-018-04693-9
- Anomalous Reactivity of Silylborane: Transition-Metal-Free Boryl Substitution of Aryl, Alkenyl, and Alkyl Halides with Silylborane/Alkoxy Base Systems
Yamamoto, E.; Izumi, K.; Horita,Y.; Ito, H. J. Am. Chem. Soc. 2012, 134, 19997–20000.
DOI: 10.1021/ja309578k
- Copper-catalyzed γ-Selective and Stereospecific Substitution Reaction of Allylic Carbonates with Diboron: Efficient Route to Chiral Allylboron Compounds
Ito, H.; Kawakami, C.; Sawamura, M. J. Am. Chem. Soc. 2005, 127, 16034–16035.
DOI: 10.1021/ja056099x
- Boration of an α,β-Enone Using a Diboron Promoted by a Copper(I)-Phosphine Mixture Catalyst.
Ito, H.; Yamanaka, H.; Tateiwa, J.-i.; Hosomi, A. Tetrahedron Lett. 2000, 41, 6821–6825.
DOI: 10.1016/S0040-4039(00)01161-8
- New Method for Introduction of a Silyl Group into α,β-Enones using a Disilane Catalyzed by a Copper(I) Salt.
Ito, H.; Ishizuka, T.; Tateiwa, J.-i.; Sonoda, M.; Hosomi, A. J. Am. Chem. Soc. 1998, 120, 11196–11197.
DOI: 10.1021/ja9822557

